添加日期:2017年11月17日 阅读:2148
10月23日,国家食品药品监管总局将《药品管理法》“修订草案”发布于**网站上对外征求意见,截止日期为10月30日。在这一版的“修订草案”中,说明为了落实国务院“放管服”要求,食品药品监管总局已按程序,报请取消药物临床试验机构资格认定、药品生产质量管理规范认证(GMP)和药品经营质量管理规范认证(GSP)3项行政审批事项。这证实了此前业界一直关注的“GMP、GSP认证制度将会被取消”所言非虚,今后将依法由上市许可持有人对药品安全、有效和质量可控承担法律责任。
这对于近年来陆续实施GMP认证时间还不算长的中药饮片产业来说,行业监管的变革影响值得关注。
据《中药饮片行业发展研究蓝皮书(2017)》调研,我国中药饮片行业市场规模将近2000亿元,在医药工业占比6.6%。随着国家宏观政策对中医药产业支持力度的加大,未来占比有望继续提升。作为用于中医临床或中成药制剂生产使用的处方药品,中药饮片的质量一方面直接关系中医临床用药安全,另一方面间接影响中成药制剂的质量。中药饮片的生产和流通一直是药品监管的重点。近几年来,监管部门不断加大对中药饮片行业的监管力度,开展了一系列专项整治行动,飞行检查趋于常态化,许多企业被要求停产整顿。但中药饮片行业暴露的问题一直没有根本上好转,违法、违规现象依然频发。
中药饮片行业监管形势依然严峻
从近年全国中药材及饮片抽验情况看,根据中国食品药品检定研究院数据,2016年全国各省、自治区和直辖市对各辖区中药材及中药饮片产品抽检共计54276批次,不合格率为23%,相比2015年降低两个百分点;2013~2016年中药材及饮片合格率呈逐年提升、稳步向好的趋势,但相对于其他类药品,中药材及饮片的不合格率依然较高。不同于其他类药品,不合格的中药材及饮片并不完全等同于“伪药”和“劣药”,水分、性状(甚至片形等)、含量等项目都可能是导致中药饮片质量不合格的原因。
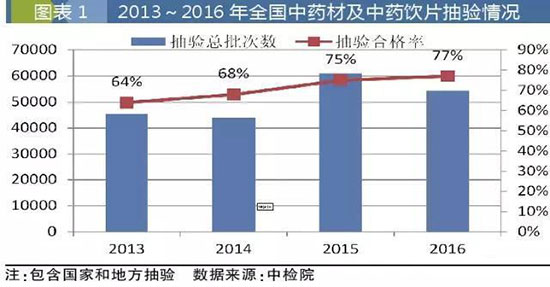
中药饮片行业产品不合格率一直居高不下,其原因是多方面的。有些是可以通过加大违规处罚力度、提升行业门槛等行政监管措施改善的,例如染色、增重、掺假、过度SO2熏蒸等人为、恶意的违规、违法行为,以及养护存储不当造成的虫蛀和霉变现象。有些则是由于中药材及饮片质量均一性差和可控性差的**属性造成的,例如部分情况的含量测定、浸出物等项目不合格,这涉及到如何科学评价中药材及饮片质量的深层次问题,是需要加大相关基础研究工作并在制定质量标准时慎重考虑的。有些是由于中药材种植不规范造成的,例如重金属、农药残留等超标现象——这些不合格现象需要通过不断提升中药材种植的规范化和规模化水平而逐步改善。同时规范化和规模化种植也可以一定程度上提升中药材及饮片的质量均一性和可控性。
认证引导中药饮片走向科学化、标准化和规范化
自2008年起,我国对中药饮片生产过程实施GMP管理,标志着数千年来以农副产品形态存在中药材及饮片开始过渡到工业产品形态的巨大转变。GMP管理是中药饮片行业走向科学化、标准化和规范化发展道路的重要里程碑。截至2017年9月底,国家及各省药监部门发放中药饮片生产GMP证书共1808张。
相对于其他类药品(无菌制剂、非无菌制剂、原料药等),中药饮片生产环节暴露的问题极其多、复杂,且难以从根本上解决。2014~2016年,CFDA不断加强医药工业企业合规监管,中药饮片企业成为GMP证书收回的“重灾区”。2016年各级药监部门共计收回172张药品生产GMP证书,其中涉及中药饮片GMP证书79张,占比高达46.2%,即2016年中药饮片全行业约5%的GMP证书被收回。有业内**认为,即便是GMP证书没被收回,超半数持证企业也一定程度上存在问题。
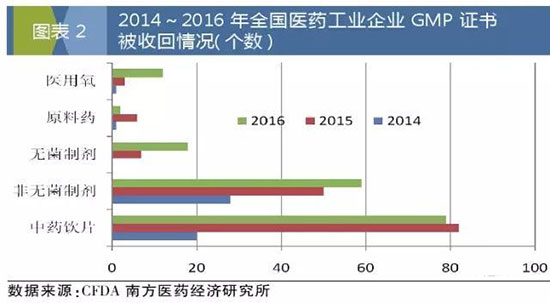
目前GMP跟踪检查出现问题比较突出的几大方面:1.非法购进中药饮片半成品或购入成品分包装,向中药材销售公司“买票”;2.中药材原料和中药饮片产品没有严格每批执行全项目检,缺少对照药材和标准品购买记录,检验记录造假等;3.生产记录造假,或没有及时记录,实际生产过程与工艺流程不符的问题也比较突出;4.虚开票据,过票,销售票据不能完全追溯;5.假冒贴牌生产等;6.车间外生产等。
中药饮片流通监管是保障中药饮片质量的*重要的环节。无论是国家及各省市层面的抽验、质量公告,还是GMP跟踪检查,监管覆盖面和力度都主要集中于拥有“两证”的合法生产企业。因此流通环节监管是发现问题产品,打击和惩处无证企业*重要的方式。
目前中药饮片违规购销现象还时常存在,例如个别医院不从中药饮片企业进货,而是违规在药材市场购买饮片;有部分医院和药店为了应付药监部门的监管,先通过正规渠道购进少量的中药饮片以获得相关资料,例如检验报告、合格证、外包装等,再从非法渠道低价购进同品种的中药饮片进行销售,由于中药饮片一般都是拆除包装放入药屉中后再进行销售和调配,这样就造成出现问题时难以确定真正违规生产厂家,甚至合规企业遭到处罚。另外,“走票过票”、挂靠经营饮片的现象较为突出。
中药饮片在医疗机构药房和零售药店终端多散放在药斗里,基本相当于直接暴露在空气中;如果养护不到位,出现质量问题的风险很高;未来需要强化医疗机构药房和零售药店保障中药饮片质量的责任意识。为了降低中药饮片在以上终端的质量风险,推行、普及小包装中药饮片很有必要。在中药饮片流通和使用环节,如何对问题产品快速有效溯源是个比较棘手的问题。加强中药饮片流通企业和使用终端的票据管理工作,有利于解决中药饮片溯源难题,是中药饮片流通管理的重点。
中药饮片监管能力有待提升
在中药饮片监管方式方面,仍过度强调政府作为监管的单一主体,监管手段过于单一,忽视其他主体的能动性,例如消费者、中成药企业和医疗机构等主体在维护中药饮片安全中的主动性。在监管力量方面,也存在不足。目前中药饮片监管专业人员特别是基层监管人力不足,且存在监管处室行政性事务过多,耗费部分专业监管力量。在执法能力方面由于中药饮片具有较强的专业性,在执法过程中急需具备中药饮片专业知识和法律背景的复合型专业人才。
中药饮片使用终端质量管理主体责任需加强。目前中药饮片没有明确、强制性的包装方面的规定,一般情况下包装规格和包装材料主要参照成药方面的规定。在医疗机构,特别是基层医疗机构小包装中药饮片普及率有待提升,“散货”仍大量存在;中药传统调配习惯难以在短期内改变,中药饮片在使用终端出现质量问题的风险很高。同时中药饮片使用终端违规从非法企业进货,或者购入一部分正品再买一部分非法产品充当正品等违规现象依然存在。中药饮片使用终端质量管理主体责任需加强。
中药饮片进入全程监管新时代
完善适合中药饮片产业特点的法律法规。不断探索和完善符合中医理论和中药饮片产业特点的法律法规体系是药品监督管理部门对中药饮片行业实施有效监管的前提和基础。
规范中药饮片流通管理。明确地方炮制规范的法律定位,针对地方炮制规范收载中药饮片品种能否在全国流通以及需要符合的条件制定明确的政策规定。鉴于目前我国中药饮片质量标准体系的现状,以及地方习用或特色品种在临床需求方面的客观事实,建议对地方炮制规范收载中药饮片品种,以中医诊疗机构和中成药企业实际市场需求为导向,可在其他省相关部门备案后,准予有限度全国流通。
研究制定中药材产地趁鲜加工政策。目前除国家允许的60多个中药材品种外,中药饮片生产企业都必须购置药材原型进行加工,即药材在进饮片生产企业之前必须符合药材标准进行干燥等,进入生产企业加工饮片的过程前,还需要润洗等,有些品种需要长时间润洗浸泡,导致有效成分含量的散失(散失到润洗的水中)。有些品种,例如郁金、预知子等,在产地不允许切片,但是在产地干燥后,然后进入生产企业后难以切片,或片型难以合格。建议扩大允许产地趁鲜加工的品种范围,允许饮片生产企业购进产地适当加工的中药饮片半成品,然后进行后续炮制步骤。
此外,建立不合格现象分级处罚制度,对恶意行为加重处罚、加快实施批准文号管理、提升监管力量/能力,提升鉴定鉴别新技术在质量管理机构中的普及率、提升监管队伍专业水平,也是中药饮片进入全程监管新时代需要大力推动的工作内容。
文章来源:
1.凡本网注明“来源:1168医药招商网”的所有作品,均为广州金孚互联网科技有限公司-1168医药招商网合法拥有版权或有权使用的作品,未经本网授权不得转载、摘编或利用其它方式使用上述作品。已经本网授权使用作品的,应在授权范围内使用,并注明“来源:1168医药招商网http://www.1168.tv”。违反上述声明者,本网将追究其相关法律责任。
2.本网转载并注明自其它来源(非1168医药招商网)的作品,目的在于传递更多信息,并不代表本网赞同其观点或和对其真实性负责,不承担此类作品侵权行为的直接责任及连带责任。
3.其他媒体、网站或个人从本网转载时,必须保留本网注明的作品第一来源,并自负版权等法律责任。
4.如涉及作品内容、版权等问题,请在作品发表之日起一周内与本网联系,否则视为放弃相关权利。联系邮箱:1753418380@qq.com。

【适用范围】用于缓解颈、肩、腰、腿及闭合性软组织疼痛、肿胀等不适症状人群的物理冷敷。【使用方法】外用。将本品适量直接涂抹于不适部位,轻轻按摩2-3分钟,每日2-3次。

【适用范围】用于缓解颈、肩、腰、腿及闭合性软组织疼痛、肿胀等不适症状人群的物理冷敷。【使用方法】外用。将本品适量直接涂抹于不适部位,轻轻按摩2-3分钟,每日2-3次。
 粤公网安备 44011102000390号
粤公网安备 44011102000390号